Laboratorio Nº1 de Fundamentos de Microbiología
Observación de Bacterias
Tinción Simple
Introducción
Las bacterias son microorganismos que, debido a su reducido tamaño y la falta de pigmentación natural, son transparentes al microscopio óptico estándar. Por esta razón, la microbiología depende de técnicas de contraste como la tinción para hacer visibles estas estructuras celulares. El presente trabajo se enmarca en la necesidad de dominar las técnicas básicas de visualización celular.
La Tinción Simple es una técnica fundamental que emplea un único colorante básico (generalmente con carga positiva, como el Azul de Metileno) para reaccionar con los componentes cargados negativamente de la célula bacteriana, como la pared celular y el citoplasma. El objetivo de este procedimiento es aumentar el contraste para poder determinar la morfología (forma: cocos, bacilos, espirilos) y la agrupación de las bacterias.
La investigación se ha puesto en marcha para aplicar estos fundamentos teóricos a la práctica, utilizando muestras de la vida cotidiana (yogur, sarro dental y vinagre de manzana) que albergan poblaciones microbianas diversas. La información previa indica que estas muestras contendrán bacterias lácticas, flora mixta oral y bacterias acéticas, respectivamente, permitiendo un estudio comparativo de las distintas morfologías y sus patrones de crecimiento.
Objetivos
-
Realizar una tinción simple de bacterias procedentes de distintas muestras naturales.
-
Realizar dos tipos de fijaciones bacterianas y saber en qué casos se recomienda una u otra.
-
Observar la morfología bacteriana y aprender a distinguir los distintos tipos de agrupaciones que existen.
-
Practicar con el microscopio al máximo aumento y con el correcto empleo del aceite de inmersión.
Materiales
-
Mechero de Alcohol
-
Fósforos o Encendedor
-
Asa Bacteriológica
-
Pinza de Madera
-
Portaobjetos
-
Microscopio
-
Soporte de Tinción
-
Muestras Bacterianas de Origen Natural: Yogur, Sarro Dental y Vinagre de Manzana
-
Colorante para Tinción: Azul de Metileno al 1%
-
Aceite de Inmersión
-
Goteros
Metodología
a. Bacterias del Yogur
Se esterilizó el asa bacteriológica por incineración al colocarla en la llama del mechero de alcohol hasta que se puso al rojo vivo y, posteriormente, se dejó enfriar brevemente antes de tomar la muestra de yogur.
Se depositó una pequeña gota de agua destilada sobre un portaobjeto. A continuación, se tomó una mínima porción de yogur con el asa bacteriológica, que ya estaba esterilizada. Esta porción de yogur se mezcló con la gota de agua y se extendió sobre la superficie del portaobjeto para crear una capa fina y uniforme.

Adicionalmente, se preparó otra muestra utilizando un segundo portaobjeto como herramienta de extensión.

Se procedió a la fijación de las muestras al calor pasando el portaobjeto rápidamente por la llama del mechero (sin exponer la muestra directamente a la llama), con la única finalidad de secar completamente y fijar las bacterias a la superficie del portaobjetos.

Los portaobjetos se apoyaron sobre el soporte de tinciones. Se añadieron unas gotas de azul de metileno hasta cubrir completamente el frotis y se dejó actuar durante 4 a 5 minutos para que el colorante penetrara en las células bacterianas.

Una vez transcurrido el tiempo de tinción, se tomó la botella de agua destilada y se procedió a lavar cuidadosamente el portaobjeto. Para ello, se inclinó ligeramente el portaobjeto y se comenzó a verter agua sobre la muestra, permitiendo que el agua escurriera y arrastrara el exceso de colorante.

Se agregó alcohol a la muestra, dejándolo actuar aproximadamente 2 minutos con el propósito de desengrasar el frotis. Posteriormente, la muestra se lavó nuevamente con agua destilada para asegurar la retirada completa del alcohol. Finalmente, la muestra se secó con el calor del mechero, pasándola rápidamente a través de la llama, para dejarla lista para la observación microscópica.
Se realizó la observación inicial utilizando el objetivo de 10x y posteriormente el de 40x para localizar la muestra y enfocarla. Para la observación de máximo detalle, se giró el revóolver, se depositó una pequeña gota de aceite de inmersión directamente sobre el frotis, y se procedió a observar con el objetivo de 100x.

b. Bacterias del Sarro Dental
Se utilizó un hisopo estéril que fue humedecido ligeramente con agua destilada. Este hisopo se pasó suavemente por la encía de un compañero voluntario para recolectar la flora bacteriana. El hisopo con la muestra recolectada se puso en contacto con el portaobjeto. Y luego se depositó una pequeña gota de agua destilada sobre el portaobjeto. A continuación, con el asa bacteriológica (previamente esterilizada), se comenzó a mezclar la muestra con la gota de agua y se extendió sobre la superficie del portaobjeto.

Posteriormente, se procedió a la fijación de la muestra al calor pasando el portaobjeto rápidamente por la llama del mechero (sin exponer la muestra directamente a la llama), con la única finalidad de secar completamente y fijar las bacterias a la superficie del portaobjetos.

El portaobjeto se apoyó sobre el soporte de tinciones. Se añadieron unas gotas de azul de metileno hasta cubrir completamente el frotis y se dejó actuar durante 4 a 5 minutos para que el colorante penetrara en las células bacterianas.

Una vez transcurrido el tiempo de tinción, se tomó la botella de agua destilada y se procedió a lavar cuidadosamente el portaobjeto. Para ello, se inclinó ligeramente el portaobjeto y se comenzó a verter agua sobre la muestra, permitiendo que el agua escurriera y arrastrara el exceso de colorante.

Finalmente, la muestra se secó con el calor del mechero, pasándola rápidamente a través de la llama, para dejarla lista para la observación microscópica.

Se realizó la observación inicial utilizando el objetivo de 10x y posteriormente el de 40x para localizar la muestra y enfocarla. Para la observación de máximo detalle, se giró el revóolver, se depositó una pequeña gota de aceite de inmersión directamente sobre el frotis, y se procedió a observar con el objetivo de 100x.

c. Bacterias del Vinagre de Manzana
Se tomó con el asa bacteriológica una pequeña porción de vinagre de manzana. Esta muestra se colocó sobre un portaobjeto. Inmediatamente, se depositó una gota de agua destilada junto a la muestra. La muestra recolectada se extendió sobre el portaobjetos, mezclándose con la gota de agua. Finalmente, se procedió a la fijación de la muestra al calor pasando el portaobjeto rápidamente por la llama del mechero, con la finalidad de secar completamente y adherir las bacterias a la superficie del vidrio.

El portaobjeto se apoyó sobre el soporte de tinciones. Se añadieron unas gotas de azul de metileno hasta cubrir completamente el frotis y se dejó actuar durante 4 a 5 minutos para que el colorante penetrara en las células bacterianas.

Una vez transcurrido el tiempo de tinción, se procedió a lavar cuidadosamente el portaobjeto con agua destilada para arrastrar el exceso de colorante. Finalmente, la muestra se secó rápidamente con el calor del mechero.

Se realizó la observación inicial utilizando el objetivo de 10x y posteriormente el de 40x para localizar la muestra y enfocarla. Para la observación de máximo detalle, se giró el revóolver, se depositó una pequeña gota de aceite de inmersión directamente sobre el frotis, y se procedió a observar con el objetivo de 100x.

Resultados
A continuación, se resumen los hallazgos microscópicos obtenidos tras la tinción simple con Azul de Metileno de cada una de las muestras.
Bacterias del Yogur
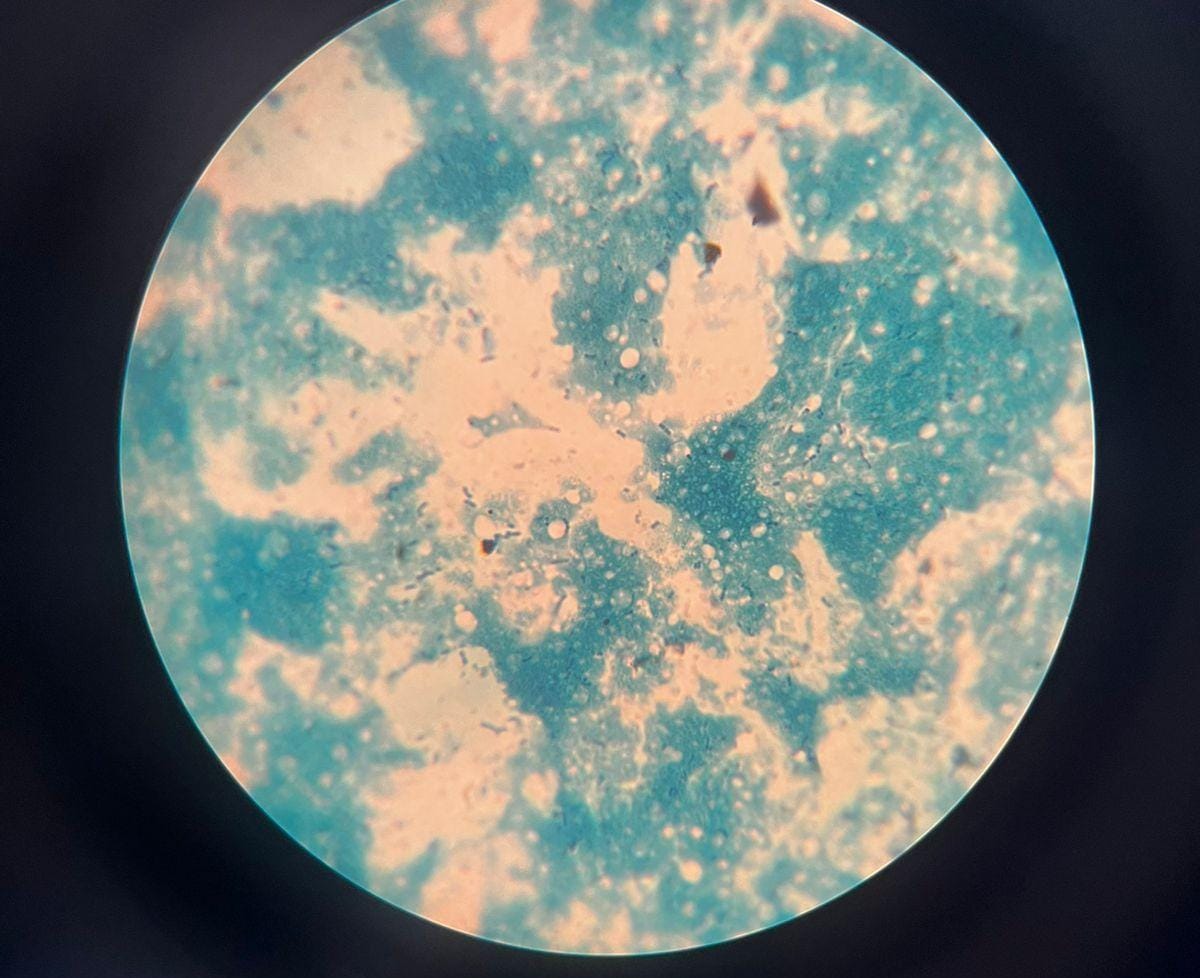
Morfologías Predominante:
- Cocos (Esferas): Estas son las bacterias redondeadas. Corresponden al Streptococcus thermophilus. En la imagen se aprecian algunas estructuras pequeñas, puntuales y de forma esférica.
- Bacilos (Bastones): Estas son las bacterias con forma de bastón o cilindro. Corresponden al Lactobacillus bulgaricus. En el fondo de la imagen, entre las áreas de color, se pueden intuir algunas formas más grandes y alargadas, que coinciden con la descripción del lactobacilo.
Agrupaciones:
- Estreptococos (Cocos en cadena): Es la agrupación típica del Streptococcus thermophilus. El término "estreptococos" significa que los cocos se agrupan en cadenas. La bacteria crece así después de la división celular.
- Bacilos aislados o en cadenas cortas: El Lactobacillus bulgaricus tiende a aparecer como bacilos individuales o formando cadenas cortas.
Bacterias del Sarro Dental
Morfología Predominante:
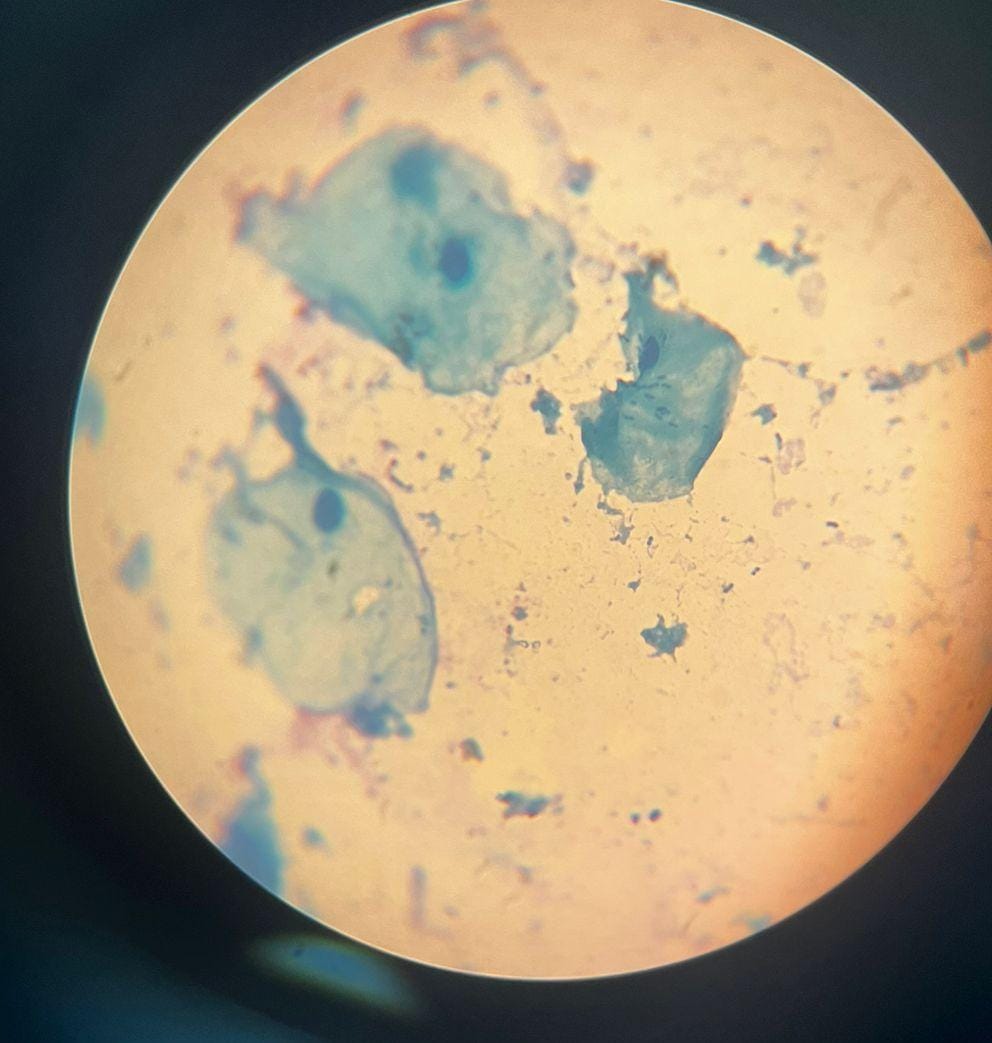
- Células Epiteliales: Aunque no son bacterias, son la estructura más dominante. Son células planas, grandes e irregulares de color azul claro, con un núcleo discernible. Indican la procedencia de la muestra bucal.
- Cocobacilos/Bacilos pequeños: Hay muchas estructuras puntuales y muy pequeñas, algunas con una forma ligeramente alargada (bastones muy pequeños o cocobacilos), esparcidas por todo el campo, especialmente en las áreas claras. Estos serían los bacilos y cocobacilos.
- Diplococos: También se pueden intuir algunos puntos muy pequeños que aparecen emparejados (diplococos).
Agrupaciones:
- Aisladas y Dispersas: Muchas de las formas bacterianas (cocos y bacilos) se ven individuales y muy dispersas alrededor del material de fondo.
- Asociaciones Cortas: Es posible intuir algunos diplococos (cocos en parejas) y cadenas cortas de bacilos o cocos.
Bacterias del Vinagre
Morfología Predominante:
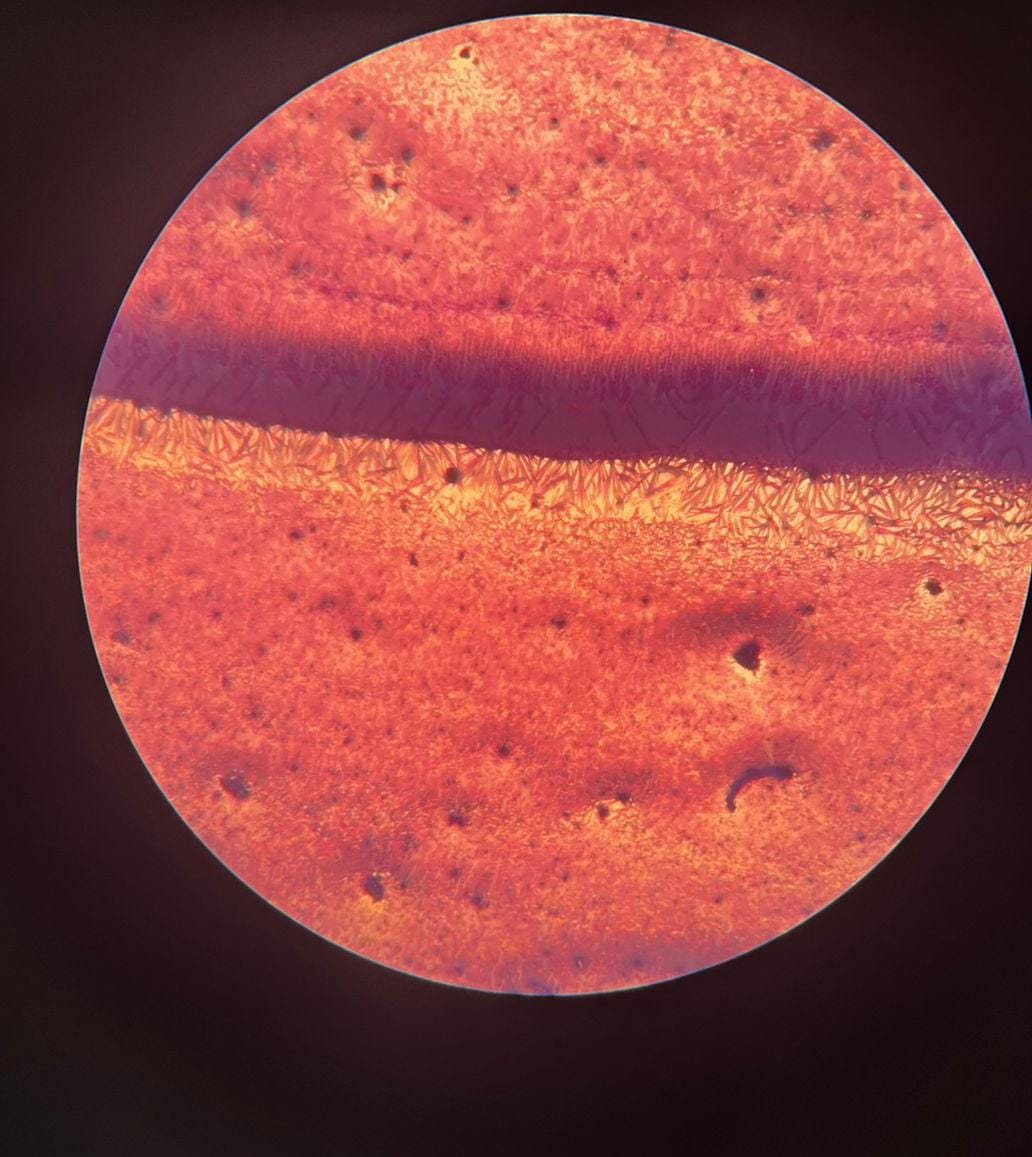
- Bacilos (Bastones): La estructura principal que domina en la banda central se compone de innumerables formas alargadas. Estos son los bacilos rectos, probablemente la bacteria Acetobacter.
Agrupaciones:
- Agrupaciones en Cadena/Filamento: Dentro de esa banda central, se observan los bacilos tan densamente empaquetados y entrelazados que parecen formar cadenas, filamentos o estructuras ramificadas. Esta alta organización es consistente con la producción de la "madre del vinagre".
Análisis y Discusión
Bacterias del Yogur:
La identificación simultánea de la morfología Cocos en cadenas (Estreptococos) y Bacilos aislados/cortos es la evidencia directa de una fermentación láctica dual y simbiótica.
La presencia de estas dos morfologías y agrupaciones confirma la acción de las cepas iniciadoras:
- La morfología de Bacilo corresponde al Lactobacillus bulgaricus, el principal responsable de la alta acidez del yogur.
- La morfología de Estreptococo corresponde al Streptococcus thermophilus, que contribuye inicialmente a la acidez y es crucial para el perfil aromático.
El resultado demuestra la efectividad del inóculo industrial, donde cada especie prospera en el medio para generar las características fisicoquímicas del producto final.
Bacterias del Sarro Dental:
La muestra revela una alta heterogeneidad de morfologías (Cocos y Bacilos/Cocobacilos) dispersas en una matriz, lo cual es altamente significativo.
Esta variedad no se debe a un inóculo único, sino que es el reflejo de la flora polimicrobiana y saprófita de la cavidad bucal. Las diferentes morfologías confirman la presencia de varios géneros bacterianos que coexisten.
La dispersión y el anclaje de estas bacterias en la muestra y la ausencia de grandes agrupaciones ordenadas confirma la estructura de una biopelícula (placa dental). El sarro es una capa densa donde las bacterias se adhieren a una matriz extracelular (glicocálix) de restos proteicos, lo que dificulta su eliminación mecánica. [attachment_0](attachment)
Bacterias del Vinagre:
La observación de la morfología Bacilar organizada en una película densa y filamentosa es la interpretación clave del proceso de acetificación.
La forma de Bacilo identifica al género Acetobacter o Gluconobacter, las bacterias aeróbicas responsables de oxidar el etanol a ácido acético.
La formación de una estructura gruesa y continua (el "velo" o "madre del vinagre") no es una simple agrupación al azar, sino una adaptación ecológica esencial. Al ser organismos aerobios obligados, las bacterias se organizan en la interfase aire-líquido para maximizar su acceso al oxígeno, lo que impulsa eficientemente la reacción de producción de vinagre.
Conclusiones
- El objetivo principal de realizar la tinción simple de bacterias se cumplió con éxito en las tres muestras. La técnica de Tinción y Visualización permitió contrastar eficazmente las células, que de otra forma serían invisibles, y obtener micrografías de alta calidad que confirman la presencia microbiana.
- En cuanto a la Fijación, se implementó y evaluó la técnica por calor para las tres muestras. Se concluye que esta fijación es rápida y efectiva para adherir bacterias al portaobjetos, un paso indispensable para evitar el arrastre celular durante el proceso de tinción y lavado.
- Respecto a la Morfología y Agrupación, se logró el objetivo de observar y distinguir estos patrones bacterianos. Se identificaron claramente cocos y bacilos, tanto en formas aisladas como en patrones específicos (estreptococos en yogur, bacilos filamentosos en vinagre y flora mixta en sarro), lo cual está directamente correlacionado con el tipo de ecosistema microbiano de cada muestra.
- Finalmente, en relación con el Dominio Microscópico, se practicó satisfactoriamente el uso del microscopio al máximo aumento, lo que incluye el correcto empleo del aceite de inmersión.